"혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구"의 두 판 사이의 차이
(제목 수정) |
(관련 정보 추가) |
||
| 212번째 줄: | 212번째 줄: | ||
* 지정범위 및 분류체계 (혁신의료기기군 지정 등에 관한 규정, ’20.6.1 시행) | * 지정범위 및 분류체계 (혁신의료기기군 지정 등에 관한 규정, ’20.6.1 시행) | ||
* 혁신의료기기군 분류(시행령 제14조)<br /> | * 혁신의료기기군 분류(시행령 제14조)<br /> | ||
| + | 관련 정보 | ||
| + | |||
| + | (KOS 메타정보) | ||
| + | |||
| + | (결과보고서) | ||
==분류 정보== | ==분류 정보== | ||
2024년 9월 19일 (목) 06:29 판
| ID | RFP-1-003 |
|---|---|
| KOS 유형 | 분류체계 |
| 수요기관 | 한국보건산업진흥원 |
| 사업년도 | 2020 |
| 기간 및 예산 | 9개월 150,000천원 |
| 공고기관 | 조달청 충북지방조달청 |
| 관련 KOS | 혁신의료기기군 분류 |
사업 개요
사업명
혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구
사업배경
의료기기산업법 시행(‘20.5)에 따른 혁신의료기기 지정 제도 운영(법 제20조, 제21조)을 위해 혁신의료기기군 지정 고시에 필요한 세부 군 분류체계 및 분류기준 마련 필요
사업목적
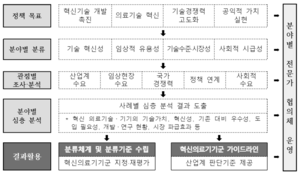
- 혁신의료기기군 지정 및 재평가 고시 제·개정에 필요한 세부 분류체계 및 분류기준 마련
- 산업계의 제도 이해도 제고를 위해 혁신의료기기군 분류체계에 따른 지정 대상, 판단기준 등 세부사항을 가이드라인으로 제시
사업기간 및 예산
- 사업기간 : 계약체결일로부터 ∼ 2020년 11월 30일까지
- 소요예산 : 150,000,000원(VAT 포함)
사업 내용
과업 내용
ㅇ 혁신의료기기군 분야별 분류체계 및 분류기준 마련
- 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련
ㅇ 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시
- 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출
ㅇ 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영
- 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영
ㅇ (가칭) 혁신의료기기군 판단기준 가이드라인 개발
- 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련
- 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영)(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구.pdf
과업요청 상세내용
1. 혁신의료기기군 분야별 분류체계 및 분류기준 마련
○ 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련
- 정책 목표 달성 관점에 필요한 세부 분류 체계 도출
- 세부 분류 체계별 용어정의, 지정 대상 심의항목, 평가방법 도출
< 혁신의료기기군 지정 대상 분야(시행령(안) 제19조) >
| 혁신의료기기군 지정 대상 분야 |
| 1. 기술집약도가 높고 혁신속도가 빠른 첨단기술 적용 분야 |
| 2. 기존 의료기술의 획기적인 개선 또는 개선이 예상되는 분야 |
| 3. 의료기기에 적용되는 핵심기술의 개발이 시급한 분야 |
| 4. 희귀·난치성 질환 진단 및 치료 등에 있어 대체 의료기기가 부재하거나 국내 수급이 어려운 분야 |
2. 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시
○ 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출
- (산업계 수요) 산업 현장의 수요 및 혁신 기술적용 제품 개발 동향 분석
- (임상현장 수요) 임상 현장의 수요 및 의료기술 관점의 혁신 제품 동향 분석
- (사회적 수요) 공익적 가치 실현에 필요한 의료기기 수요 및 개발 동향 분석
- (국가 경쟁력) 시장 확대 유망 제품분야 국내 기술 수준 분석
- (정책 연계) 국가 R&D 사업, 정부 지원정책과 연계된 타 기술 분류 체계와 정합성 검토
- 조사된 의료기기 분야의 기술적 혁신성, 국내 기술수준, 기존 의료기술 대비 우수성, 상용화 단계, 경제적 효과, 공익성 등 분류기준에 따른 전문가 검토 실시
3. 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영
○ 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영
- 제품(임상)분야별 산업계, 의학계, 공학계, 규제 등 유관기관 전문가 자문단 구성
4. (가칭) 혁신의료기기군 판단기준 가이드라인 개발
○ 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련
○ 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영)
- 혁신의료기기군을 직관적으로 판단할 수 있는 제품사례 및 혁신기술 맵을 제시하여 제도 운영의 예측 가능성 제고
| 참고 | 혁신의료기기군·기기 지정 제도 개요(의료기기산업법) |
|---|
□ 제도 개요
① 혁신의료기기군 지정 절차(법 제20조, 시행령안 제19조)
- (혁신의료기기군) 혁신의료기기의 중분류 개념으로서 혁신분야를 분류하여 의료기기산업육성·지원 위원회 심의를 거쳐 고시(3년 주기)
- (지정 대상) 법 제20조에 따라 의료기기 연구개발 촉진, 치료법 등의 개선 등을 통한 국민 삶의 질 향상을 위한 정책 목표 달성에 필요한 분야를 구분하여 지정 대상을 분류
- 혁신의료기기 지정 절차와의 정합성과 함께 연구개발 촉진 등의 정책 목적달성까지 고려
- 혁신의료기기군에 포함되는 의료기기중 법 제2조 및 제21조에 따른 혁신의료기기 지정 기준에 부합할 경우 혁신의료기기로 지정 가능(복지부·식약처 협의 지정)
- (지정 절차 등) 혁신의료기기군을 지정하거나 재평가하여 고시할 때에는 핵심 기술의 보편화 여부와 유효기간(3년) 이내에 상용화 가능성을 종합적으로 고려야 함
- 산업계, 학계, 의료계의 수요반영을 위해 기술수요조사를 실시하여 반영할 수 있음
② 혁신의료기기 지정 신청 등(시행령안 제20조)
- (대상) 법 제20조에 따라 고시된 혁신의료기기군에 포함되는 의료기기
- (지정절차) 법 제21조에 따라 식약처장이 복지부장관과 협의하여 지정
- (지정신청) 혁신의료기기를 지정 받으려는 자는 식약처장에게 지정신청서와 개발경위, 사용방법 등에 관한 자료 및 법 제21조제2항 각 호에 해당함을 입증할 수 있는 자료를 제출하여야 함
- (지정 검토) 식약처장은 제출받은 자료를 보건복지부장관에서 송부하여 협의를 요청 하고, 보건복지부장관이 통보한 협의 의견을 고려하여 혁신의료기기 지정 여부를 결정하여야 함(30일 이내)
- (인허가 특례·지원) 법 제22조에 따른 단계별 심사·우선 심사 특례, 제24조에 따른 혁신의료기기 소프트웨어 기업인증제(허가 및 변경허가 특례), 제28조에 따른 임상시험계획서 작성 지원 등
< 혁신의료기기 지정·지원 제도 운영(안) 요약 >
| 구분 | 혁신의료기기군 지정(법 제20조 관련) | 혁신의료기기 지정(법 제21조~제24조 관련) |
|---|---|---|
| 개념 | ○ 혁신의료기기 지정 대상 기술분야를 분류 및 정의하여 고시 | ○ 혁신의료기기군에 포함되는 기술 중 법 제21조 각 호의 요건을 검토하여 지정 |
| 지정주체 | ○ 의료기기산업 육성·지원 위원회 | |
| (보건복지부장관 고시) | ○ 식품의약품안전처장(복지부장관 협의) | |
| 지정방법 | ○ 의료기기산업육성·지원위원회 심의·의결 | ○ 식품의약품안전처 검토·지정여부 결정 |
| * 필요시 전문위원회 심의 | ||
| 유효기간 | ○ 3년(재평가를 통한 연장·신규 분류 가능) | |
| - 지정분야 의료기기의 보편화 등을 고려하여 연장여부 결정 | ○ 혁신의료기기군 유효기간에 따름 | |
| 지원특례 | - | ○ 단계별심사/우선심사 등 인허가 절차상 특례 |
| ○ 혁신 소프트웨어 별도 인허가 특례 기준 적용 | ||
| ○ 임상시험 계획서 검토 지원 | ||
| 기타 지원 | ○ 혁신의료기기군 대상 기술 개발 시 정부 R&D와 연계하여 지원(종합계획 반영 검토) | ○ 혁신의료기기 안전관리 기반구축/표준화 |
| ○ 혁신의료기기 등의 사용 활성화 지원 | ||
| ○ 혁신의료기기 연구개발 및 생산기업 혁신형 인증 시 별도 기준 적용 |
ㅇ KHIDI 의료기기산업 종합정보시스템 - 혁신 의료기기•군 지정
- 혁신 의료기기•군 지정 안내 / 혁신의료기기군 분류(시행령 제14조)
- 혁신의료기기군은 의료기기산업법 제20조에 따라 의료기기 연구개발 촉진, 치료법의 획기적 개선, 희귀난치성 질환 치료 등을 고려하여 위원회 심의를 거쳐 지정되고 있습니다.
- 유효기간
- 지정일로부터 3년(3년마다 재평가를 통해 지정 연장 가능)
- 지정방법
- 지정범위 및 분류체계 (혁신의료기기군 지정 등에 관한 규정, ’20.6.1 시행)
- 혁신의료기기군 분류(시행령 제14조)
관련 정보
(KOS 메타정보)
(결과보고서)
분류 정보
| KDC6 | 373 | 학습지도, 교육방법 |
|---|---|---|
| DDC23 | 371 | Schools and their activities; special education |
| ILC | spe | education services; schools |
| BRM | 산업·통상·중소기업 > 산업진흥·고도화 | |