"혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구"의 두 판 사이의 차이
(혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구 제안서 정보) |
|||
| (다른 사용자 한 명의 중간 판 7개는 보이지 않습니다) | |||
| 1번째 줄: | 1번째 줄: | ||
| + | {{infobox | ||
| + | |title = [[혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구]] | ||
| + | |label2 = ID | ||
| + | |data2 = RFP-1-003 | ||
| + | |label4 = 수요기관 | ||
| + | |data4 = [https://www.khidi.or.kr/kps 한국보건산업진흥원] | ||
| + | |label5 = 공고기관 | ||
| + | |data5 = 조달청 충북지방조달청 | ||
| + | |label6 = 사업년도 | ||
| + | |data6 = 2020 | ||
| + | |label7 = 기간 및 예산 | ||
| + | |data7 = 9개월 150,000천원 | ||
| + | |label8 = KOS 유형 | ||
| + | |data8 =[[분류체계]] | ||
| + | |label9 = 관련 KOS | ||
| + | |data9 = 혁신의료기기군 분류 | ||
| + | }} | ||
| + | ==사업 개요== | ||
| + | |||
| + | '''사업명''' | ||
| + | |||
| + | 혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구 | ||
| + | |||
| + | '''사업배경''' | ||
| + | |||
| + | 의료기기산업법 시행(‘20.5)에 따른 혁신의료기기 지정 제도 운영(법 제20조, 제21조)을 위해 혁신의료기기군 지정 고시에 필요한 세부 군 분류체계 및 분류기준 마련 필요 | ||
| + | |||
| + | '''사업목적''' | ||
| + | |||
| + | - 혁신의료기기군 지정 및 재평가 고시 제·개정에 필요한 세부 분류체계 및 분류기준 마련 | ||
| + | |||
| + | - 산업계의 제도 이해도 제고를 위해 혁신의료기기군 분류체계에 따른 지정 대상, 판단기준 등 세부사항을 가이드라인으로 제시 | ||
| + | |||
| + | '''사업기간 및 예산''' | ||
| + | |||
| + | - 사업기간 : 계약체결일로부터 ∼ 2020년 11월 30일까지 | ||
| + | |||
| + | - 소요예산 : 150,000,000원(VAT 포함) | ||
| + | [[파일:(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구.pdf|섬네일|(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구]] | ||
| + | |||
| + | ==사업 내용== | ||
| + | |||
| + | '''과업 내용''' | ||
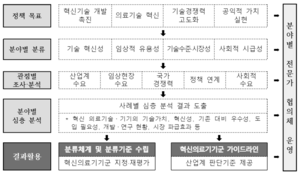
| + | [[파일:과업추진체계.png|대체글=혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구 과업추진체계|섬네일|'''과업추진체계(안)''']] | ||
| + | ㅇ 혁신의료기기군 분야별 분류체계 및 분류기준 마련 | ||
| + | |||
| + | * 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련 | ||
| + | |||
| + | ㅇ 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시 | ||
| + | |||
| + | * 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출 | ||
| + | |||
| + | ㅇ 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영 | ||
| + | |||
| + | * 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영 | ||
| + | |||
| + | ㅇ (가칭) 혁신의료기기군 판단기준 가이드라인 개발 | ||
| + | |||
| + | * 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련 | ||
| + | * 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영)[[:파일:(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구.pdf|(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구.pdf]] | ||
| + | |||
| + | |||
| + | '''과업요청 상세내용''' | ||
| + | |||
| + | '''1. 혁신의료기기군 분야별 분류체계 및 분류기준 마련''' | ||
| + | |||
| + | ○ 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련 | ||
| + | |||
| + | * 정책 목표 달성 관점에 필요한 세부 분류 체계 도출 | ||
| + | * 세부 분류 체계별 용어정의, 지정 대상 심의항목, 평가방법 도출 | ||
| + | |||
| + | |||
| + | < 혁신의료기기군 지정 대상 분야(시행령(안) 제19조) > | ||
| + | {| class="wikitable" | ||
| + | |'''혁신의료기기군 지정 대상 분야''' | ||
| + | |- | ||
| + | |1. 기술집약도가 높고 혁신속도가 빠른 첨단기술 적용 분야 | ||
| + | |- | ||
| + | |2. 기존 의료기술의 획기적인 개선 또는 개선이 예상되는 분야 | ||
| + | |- | ||
| + | |3. 의료기기에 적용되는 핵심기술의 개발이 시급한 분야 | ||
| + | |- | ||
| + | |4. 희귀·난치성 질환 진단 및 치료 등에 있어 대체 의료기기가 부재하거나 국내 수급이 어려운 분야 | ||
| + | |} | ||
| + | |||
| + | |||
| + | '''2. 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시''' | ||
| + | |||
| + | ○ 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출 | ||
| + | |||
| + | * '''(산업계 수요)''' 산업 현장의 수요 및 혁신 기술적용 제품 개발 동향 분석 | ||
| + | * '''(임상현장 수요)''' 임상 현장의 수요 및 의료기술 관점의 혁신 제품 동향 분석 | ||
| + | * '''(사회적 수요)''' 공익적 가치 실현에 필요한 의료기기 수요 및 개발 동향 분석 | ||
| + | * '''(국가 경쟁력)''' 시장 확대 유망 제품분야 국내 기술 수준 분석 | ||
| + | * '''(정책 연계)''' 국가 R&D 사업, 정부 지원정책과 연계된 타 기술 분류 체계와 정합성 검토 | ||
| + | |||
| + | * 조사된 의료기기 분야의 기술적 혁신성, 국내 기술수준, 기존 의료기술 대비 우수성, 상용화 단계, 경제적 효과, 공익성 등 분류기준에 따른 전문가 검토 실시 | ||
| + | |||
| + | |||
| + | '''3. 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영''' | ||
| + | |||
| + | ○ 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영 | ||
| + | |||
| + | * 제품(임상)분야별 산업계, 의학계, 공학계, 규제 등 유관기관 전문가 자문단 구성 | ||
| + | |||
| + | |||
| + | '''4. (가칭) 혁신의료기기군 판단기준 가이드라인 개발''' | ||
| + | |||
| + | ○ 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련 | ||
| + | |||
| + | ○ 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영) | ||
| + | |||
| + | * 혁신의료기기군을 직관적으로 판단할 수 있는 제품사례 및 혁신기술 맵을 제시하여 제도 운영의 예측 가능성 제고 | ||
| + | |||
| + | {| class="wikitable" | ||
| + | !참고 | ||
| + | !혁신의료기기군·기기 지정 제도 개요(의료기기산업법) | ||
| + | |} | ||
| + | □ 제도 개요 | ||
| + | |||
| + | ① '''혁신의료기기군 지정 절차'''(법 제20조, 시행령안 제19조) | ||
| + | |||
| + | * '''(혁신의료기기군)''' 혁신의료기기의 중분류 개념으로서 혁신분야를 분류하여 의료기기산업육성·지원 위원회 심의를 거쳐 고시(3년 주기) | ||
| + | * '''(지정 대상)''' 법 제20조에 따라 의료기기 연구개발 촉진, 치료법 등의 개선 등을 통한 국민 삶의 질 향상을 위한 정책 목표 달성에 필요한 분야를 구분하여 지정 대상을 분류 | ||
| + | |||
| + | * 혁신의료기기 지정 절차와의 정합성과 함께 연구개발 촉진 등의 정책 목적달성까지 고려 | ||
| + | |||
| + | * 혁신의료기기군에 포함되는 의료기기중 법 제2조 및 제21조에 따른 혁신의료기기 지정 기준에 부합할 경우 혁신의료기기로 지정 가능(복지부·식약처 협의 지정) | ||
| + | |||
| + | * '''(지정 절차 등)''' 혁신의료기기군을 지정하거나 재평가하여 고시할 때에는 핵심 기술의 보편화 여부와 유효기간(3년) 이내에 상용화 가능성을 종합적으로 고려야 함 | ||
| + | |||
| + | * 산업계, 학계, 의료계의 수요반영을 위해 기술수요조사를 실시하여 반영할 수 있음 | ||
| + | |||
| + | ② '''혁신의료기기 지정 신청 등'''(시행령안 제20조) | ||
| + | |||
| + | * '''(대상)''' 법 제20조에 따라 고시된 혁신의료기기군에 포함되는 의료기기 | ||
| + | * '''(지정절차)''' 법 제21조에 따라 식약처장이 복지부장관과 협의하여 지정 | ||
| + | |||
| + | * '''(지정신청)''' 혁신의료기기를 지정 받으려는 자는 식약처장에게 지정신청서와 개발경위, 사용방법 등에 관한 자료 및 법 제21조제2항 각 호에 해당함을 입증할 수 있는 자료를 제출하여야 함 | ||
| + | * '''(지정 검토)''' 식약처장은 제출받은 자료를 보건복지부장관에서 송부하여 협의를 요청 하고, 보건복지부장관이 통보한 협의 의견을 고려하여 혁신의료기기 지정 여부를 결정하여야 함(30일 이내) | ||
| + | * '''(인허가 특례·지원)''' 법 제22조에 따른 단계별 심사·우선 심사 특례, 제24조에 따른 혁신의료기기 소프트웨어 기업인증제(허가 및 변경허가 특례), 제28조에 따른 임상시험계획서 작성 지원 등 | ||
| + | |||
| + | |||
| + | < 혁신의료기기 지정·지원 제도 운영(안) 요약 > | ||
| + | {| class="wikitable" | ||
| + | !'''구분''' | ||
| + | !'''혁신의료기기군 지정(법 제20조 관련)''' | ||
| + | !'''혁신의료기기 지정(법 제21조~제24조 관련)''' | ||
| + | |- | ||
| + | |개념 | ||
| + | |○ 혁신의료기기 지정 대상 기술분야를 분류 및 정의하여 고시 | ||
| + | |○ 혁신의료기기군에 포함되는 기술 중 법 제21조 각 호의 요건을 검토하여 지정 | ||
| + | |- | ||
| + | |지정주체 | ||
| + | |○ 의료기기산업 육성·지원 위원회 | ||
| + | | | ||
| + | |- | ||
| + | |(보건복지부장관 고시) | ||
| + | |○ 식품의약품안전처장(복지부장관 협의) | ||
| + | | | ||
| + | |- | ||
| + | |지정방법 | ||
| + | |○ 의료기기산업육성·지원위원회 심의·의결 | ||
| + | |○ 식품의약품안전처 검토·지정여부 결정 | ||
| + | |- | ||
| + | |* 필요시 전문위원회 심의 | ||
| + | | | ||
| + | | | ||
| + | |- | ||
| + | |유효기간 | ||
| + | |○ 3년(재평가를 통한 연장·신규 분류 가능) | ||
| + | | | ||
| + | |- | ||
| + | | - 지정분야 의료기기의 보편화 등을 고려하여 연장여부 결정 | ||
| + | |○ 혁신의료기기군 유효기간에 따름 | ||
| + | | | ||
| + | |- | ||
| + | |지원특례 | ||
| + | | - | ||
| + | |○ 단계별심사/우선심사 등 인허가 절차상 특례 | ||
| + | |- | ||
| + | |○ 혁신 소프트웨어 별도 인허가 특례 기준 적용 | ||
| + | | | ||
| + | | | ||
| + | |- | ||
| + | |○ 임상시험 계획서 검토 지원 | ||
| + | | | ||
| + | | | ||
| + | |- | ||
| + | |기타 지원 | ||
| + | |○ 혁신의료기기군 대상 기술 개발 시 정부 R&D와 연계하여 지원(종합계획 반영 검토) | ||
| + | |○ 혁신의료기기 안전관리 기반구축/표준화 | ||
| + | |- | ||
| + | |○ 혁신의료기기 등의 사용 활성화 지원 | ||
| + | | | ||
| + | | | ||
| + | |- | ||
| + | |○ 혁신의료기기 연구개발 및 생산기업 혁신형 인증 시 별도 기준 적용 | ||
| + | | | ||
| + | | | ||
| + | |} | ||
| + | |||
| + | |||
| + | ㅇ [https://www.khidi.or.kr/board?menuId=MENU02616&siteId=SITE00004 KHIDI 의료기기산업 종합정보시스템 - 혁신 의료기기•군 지정] | ||
| + | |||
| + | * 혁신 의료기기•군 지정 안내 / 혁신의료기기군 분류(시행령 제14조) | ||
| + | * 혁신의료기기군은 의료기기산업법 제20조에 따라 의료기기 연구개발 촉진, 치료법의 획기적 개선, 희귀난치성 질환 치료 등을 고려하여 위원회 심의를 거쳐 지정되고 있습니다. | ||
| + | * 유효기간 | ||
| + | * 지정일로부터 3년(3년마다 재평가를 통해 지정 연장 가능) | ||
| + | * 지정방법 | ||
| + | * 지정범위 및 분류체계 (혁신의료기기군 지정 등에 관한 규정, ’20.6.1 시행) | ||
| + | * 혁신의료기기군 분류(시행령 제14조)<br /> | ||
| + | |||
| + | ==관련 정보== | ||
| + | |||
| + | (KOS 메타정보) | ||
| + | |||
| + | (결과보고서) | ||
| + | |||
| + | ==분류 정보== | ||
| + | {| class="wikitable" | ||
| + | |- | ||
| + | ![http://openarchives.net/kos/%EB%B6%84%EB%A5%98:KDC KDC6] | ||
| + | |[http://openarchives.net/kos/%EB%B6%84%EB%A5%98:373(KDC) 373]||학습지도, 교육방법 | ||
| + | |- | ||
| + | ![http://openarchives.net/kos/%EB%B6%84%EB%A5%98:DDC DDC23] | ||
| + | |[http://openarchives.net/kos/%EB%B6%84%EB%A5%98:371(DDC) 371]||Schools and their activities; special education | ||
| + | |- | ||
| + | !ILC | ||
| + | |[http://openarchives.net/kos/%EB%B6%84%EB%A5%98:Spe(ILC) spe]||education services; schools | ||
| + | |- | ||
| + | ! BRM | ||
| + | | colspan="2" |[http://openarchives.net/kos/%EB%B6%84%EB%A5%98:%EC%82%B0%EC%97%85%C2%B7%ED%86%B5%EC%83%81%C2%B7%EC%A4%91%EC%86%8C%EA%B8%B0%EC%97%85(BRM1:%EC%A0%95%EC%B1%85%EB%B6%84%EC%95%BC) 산업·통상·중소기업] > [http://openarchives.net/kos/%EB%B6%84%EB%A5%98:%EC%82%B0%EC%97%85%EC%A7%84%ED%9D%A5%C2%B7%EA%B3%A0%EB%8F%84%ED%99%94(BRM2:%EC%A0%95%EC%B1%85%EC%98%81%EC%97%AD) 산업진흥·고도화] | ||
| + | |} | ||
| + | |||
| + | ==외부 링크== | ||
| + | *[https://www.khidi.or.kr/board/view?pageNum=1&rowCnt=20&no1=1&linkId=48848180&refMenuId=MENU01499&menuId=MENU01498&maxIndex=&minIndex=&schType=1&schText=혁신의료기기군 지정 검토 절차 안내서 발간&schStartDate=&schEndDate=&boardStyle=&categoryId=&continent=&country= 혁신의료기기군 지정 제도 안내서 링크(2020.12.01)] | ||
| + | * | ||
| + | |||
| + | [[Category: 지식구조체계]] | ||
| + | [[Category: 통계분류포털]] | ||
| + | [[Category: 분류체계]] | ||
| + | [[Category: 373(KDC)]] | ||
| + | [[Category: 371(DDC)]] | ||
| + | [[Category: spe(ILC)]] | ||
| + | [[Category: 산업·통상·중소기업(BRM1:정책분야)]] | ||
| + | [[Category: 산업진흥·고도화(BRM2:정책영역)]] | ||
2024년 9월 19일 (목) 06:42 기준 최신판
| ID | RFP-1-003 |
|---|---|
| 수요기관 | 한국보건산업진흥원 |
| 공고기관 | 조달청 충북지방조달청 |
| 사업년도 | 2020 |
| 기간 및 예산 | 9개월 150,000천원 |
| KOS 유형 | 분류체계 |
| 관련 KOS | 혁신의료기기군 분류 |
사업 개요[편집 | 원본 편집]
사업명
혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구
사업배경
의료기기산업법 시행(‘20.5)에 따른 혁신의료기기 지정 제도 운영(법 제20조, 제21조)을 위해 혁신의료기기군 지정 고시에 필요한 세부 군 분류체계 및 분류기준 마련 필요
사업목적
- 혁신의료기기군 지정 및 재평가 고시 제·개정에 필요한 세부 분류체계 및 분류기준 마련
- 산업계의 제도 이해도 제고를 위해 혁신의료기기군 분류체계에 따른 지정 대상, 판단기준 등 세부사항을 가이드라인으로 제시
사업기간 및 예산
- 사업기간 : 계약체결일로부터 ∼ 2020년 11월 30일까지
- 소요예산 : 150,000,000원(VAT 포함)
사업 내용[편집 | 원본 편집]
과업 내용
ㅇ 혁신의료기기군 분야별 분류체계 및 분류기준 마련
- 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련
ㅇ 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시
- 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출
ㅇ 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영
- 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영
ㅇ (가칭) 혁신의료기기군 판단기준 가이드라인 개발
- 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련
- 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영)(제안요청서)혁신의료기기군 분류체계 및 분류기준 가이드라인 개발 연구.pdf
과업요청 상세내용
1. 혁신의료기기군 분야별 분류체계 및 분류기준 마련
○ 법령에 제시된 정책 목표별 세부 분류체계 및 분류기준 마련
- 정책 목표 달성 관점에 필요한 세부 분류 체계 도출
- 세부 분류 체계별 용어정의, 지정 대상 심의항목, 평가방법 도출
< 혁신의료기기군 지정 대상 분야(시행령(안) 제19조) >
| 혁신의료기기군 지정 대상 분야 |
| 1. 기술집약도가 높고 혁신속도가 빠른 첨단기술 적용 분야 |
| 2. 기존 의료기술의 획기적인 개선 또는 개선이 예상되는 분야 |
| 3. 의료기기에 적용되는 핵심기술의 개발이 시급한 분야 |
| 4. 희귀·난치성 질환 진단 및 치료 등에 있어 대체 의료기기가 부재하거나 국내 수급이 어려운 분야 |
2. 혁신의료기기군 분류체계별 지정 검토 대상 의료기기 사례 제시
○ 기술수요 조사 및 기술동향 분석을 통한 분류별 예상 제품군 도출
- (산업계 수요) 산업 현장의 수요 및 혁신 기술적용 제품 개발 동향 분석
- (임상현장 수요) 임상 현장의 수요 및 의료기술 관점의 혁신 제품 동향 분석
- (사회적 수요) 공익적 가치 실현에 필요한 의료기기 수요 및 개발 동향 분석
- (국가 경쟁력) 시장 확대 유망 제품분야 국내 기술 수준 분석
- (정책 연계) 국가 R&D 사업, 정부 지원정책과 연계된 타 기술 분류 체계와 정합성 검토
- 조사된 의료기기 분야의 기술적 혁신성, 국내 기술수준, 기존 의료기술 대비 우수성, 상용화 단계, 경제적 효과, 공익성 등 분류기준에 따른 전문가 검토 실시
3. 혁신의료기기군 분류체계·기준 검토를 위한 정책 협의체 운영
○ 혁신의료기기군 분류체계·기준 검토, 기술 수준 분석(델파이 조사, 인터뷰 등) 등 전문분야별 자문을 위한 전문가 협의체 운영
- 제품(임상)분야별 산업계, 의학계, 공학계, 규제 등 유관기관 전문가 자문단 구성
4. (가칭) 혁신의료기기군 판단기준 가이드라인 개발
○ 혁신의료기기 지정 신청 시 필요한 혁신의료기기군 대상여부(판단기준), 제품 분류분야 등 신청인 관점에서 알기 쉬운 제도 안내서 마련
○ 혁신의료기기군 세부분류별 예상 제품군과 향후 지정 검토 기술 등 중장기 혁신 기술 맵 제시(기술동향 분석결과 반영)
- 혁신의료기기군을 직관적으로 판단할 수 있는 제품사례 및 혁신기술 맵을 제시하여 제도 운영의 예측 가능성 제고
| 참고 | 혁신의료기기군·기기 지정 제도 개요(의료기기산업법) |
|---|
□ 제도 개요
① 혁신의료기기군 지정 절차(법 제20조, 시행령안 제19조)
- (혁신의료기기군) 혁신의료기기의 중분류 개념으로서 혁신분야를 분류하여 의료기기산업육성·지원 위원회 심의를 거쳐 고시(3년 주기)
- (지정 대상) 법 제20조에 따라 의료기기 연구개발 촉진, 치료법 등의 개선 등을 통한 국민 삶의 질 향상을 위한 정책 목표 달성에 필요한 분야를 구분하여 지정 대상을 분류
- 혁신의료기기 지정 절차와의 정합성과 함께 연구개발 촉진 등의 정책 목적달성까지 고려
- 혁신의료기기군에 포함되는 의료기기중 법 제2조 및 제21조에 따른 혁신의료기기 지정 기준에 부합할 경우 혁신의료기기로 지정 가능(복지부·식약처 협의 지정)
- (지정 절차 등) 혁신의료기기군을 지정하거나 재평가하여 고시할 때에는 핵심 기술의 보편화 여부와 유효기간(3년) 이내에 상용화 가능성을 종합적으로 고려야 함
- 산업계, 학계, 의료계의 수요반영을 위해 기술수요조사를 실시하여 반영할 수 있음
② 혁신의료기기 지정 신청 등(시행령안 제20조)
- (대상) 법 제20조에 따라 고시된 혁신의료기기군에 포함되는 의료기기
- (지정절차) 법 제21조에 따라 식약처장이 복지부장관과 협의하여 지정
- (지정신청) 혁신의료기기를 지정 받으려는 자는 식약처장에게 지정신청서와 개발경위, 사용방법 등에 관한 자료 및 법 제21조제2항 각 호에 해당함을 입증할 수 있는 자료를 제출하여야 함
- (지정 검토) 식약처장은 제출받은 자료를 보건복지부장관에서 송부하여 협의를 요청 하고, 보건복지부장관이 통보한 협의 의견을 고려하여 혁신의료기기 지정 여부를 결정하여야 함(30일 이내)
- (인허가 특례·지원) 법 제22조에 따른 단계별 심사·우선 심사 특례, 제24조에 따른 혁신의료기기 소프트웨어 기업인증제(허가 및 변경허가 특례), 제28조에 따른 임상시험계획서 작성 지원 등
< 혁신의료기기 지정·지원 제도 운영(안) 요약 >
| 구분 | 혁신의료기기군 지정(법 제20조 관련) | 혁신의료기기 지정(법 제21조~제24조 관련) |
|---|---|---|
| 개념 | ○ 혁신의료기기 지정 대상 기술분야를 분류 및 정의하여 고시 | ○ 혁신의료기기군에 포함되는 기술 중 법 제21조 각 호의 요건을 검토하여 지정 |
| 지정주체 | ○ 의료기기산업 육성·지원 위원회 | |
| (보건복지부장관 고시) | ○ 식품의약품안전처장(복지부장관 협의) | |
| 지정방법 | ○ 의료기기산업육성·지원위원회 심의·의결 | ○ 식품의약품안전처 검토·지정여부 결정 |
| * 필요시 전문위원회 심의 | ||
| 유효기간 | ○ 3년(재평가를 통한 연장·신규 분류 가능) | |
| - 지정분야 의료기기의 보편화 등을 고려하여 연장여부 결정 | ○ 혁신의료기기군 유효기간에 따름 | |
| 지원특례 | - | ○ 단계별심사/우선심사 등 인허가 절차상 특례 |
| ○ 혁신 소프트웨어 별도 인허가 특례 기준 적용 | ||
| ○ 임상시험 계획서 검토 지원 | ||
| 기타 지원 | ○ 혁신의료기기군 대상 기술 개발 시 정부 R&D와 연계하여 지원(종합계획 반영 검토) | ○ 혁신의료기기 안전관리 기반구축/표준화 |
| ○ 혁신의료기기 등의 사용 활성화 지원 | ||
| ○ 혁신의료기기 연구개발 및 생산기업 혁신형 인증 시 별도 기준 적용 |
ㅇ KHIDI 의료기기산업 종합정보시스템 - 혁신 의료기기•군 지정
- 혁신 의료기기•군 지정 안내 / 혁신의료기기군 분류(시행령 제14조)
- 혁신의료기기군은 의료기기산업법 제20조에 따라 의료기기 연구개발 촉진, 치료법의 획기적 개선, 희귀난치성 질환 치료 등을 고려하여 위원회 심의를 거쳐 지정되고 있습니다.
- 유효기간
- 지정일로부터 3년(3년마다 재평가를 통해 지정 연장 가능)
- 지정방법
- 지정범위 및 분류체계 (혁신의료기기군 지정 등에 관한 규정, ’20.6.1 시행)
- 혁신의료기기군 분류(시행령 제14조)
관련 정보[편집 | 원본 편집]
(KOS 메타정보)
(결과보고서)
분류 정보[편집 | 원본 편집]
| KDC6 | 373 | 학습지도, 교육방법 |
|---|---|---|
| DDC23 | 371 | Schools and their activities; special education |
| ILC | spe | education services; schools |
| BRM | 산업·통상·중소기업 > 산업진흥·고도화 | |